La "Medsafetyweek", campagne mondiale de sensibilisation à la pharmacovigilance a eu lieu la semaine du 1er au 7 novembre 2021.
A cette occasion, il nous a semblé intéressant de faire un point sur l'ANSM, Agence nationale de sécurité du médicament et des produits de santé.
Quel est son rôle ?
L’ANSM est l’acteur public qui permet, au nom de l’État, l’accès aux produits de santé en France et qui assure leur sécurité tout au long de leur cycle de vie. Au cœur du système de santé, elle agit au service des patients et de leur sécurité, aux côtés des professionnels de santé et en concertation avec leurs représentants respectifs.
Elle favorise l’accès à des produits innovants via des procédures d’autorisation adaptées à chaque stade de la vie du médicament avant et après sa mise sur le marché.
Au travers de ses évaluations, ses expertises et sa politique de surveillance, elle s'assure que les produits de santé disponibles en France soient sûrs, efficaces, accessibles et bien utilisés.
L'ANSM a différentes missions :
- Surveiller les médicaments
- Surveiller les dispositifs médicaux et autres produits
- Organiser les vigilances
- Controler la qualité des produits
- Inspecter les produits et les pratiques
- Assurer la disponibilité
La pharmacovigilance
La pharmacovigilance s’exerce sur tous les médicaments utilisés par les patients en France. Elle s’intéresse aux effets indésirables survenant dans les conditions normales d’utilisation du médicament, mais aussi aux effets indésirables survenant dans le cadre d’erreurs médicamenteuses, d’abus, de mésusages, de surdosages et d’expositions professionnelles. Elle a pour but la surveillance, l'évaluation, la prévention et la gestion du risque d'effets indésirables liés à l'usage des médicaments.
Cette année, la "Medsafetyweek" avait pour thème la vaccination et pour but d'encourager la population, que ce soit les professionnels de santé ou le grand public, à reconnaître et à signaler les éventuels problèmes rencontrés avec les vaccins, notamment les vaccins contre la COVID-19.
Mais qu'elle soit liée à un vaccin, un médicament ou un produit de santé, chaque déclaration compte ! Elles permettent d'identifier d'éventuels effets indésirables rares non détectés dans le cadre des essais cliniques et d'obtenir davantage d'informations sur les effets déjà identifiés. Grâce à ces déclarations, il devient possible de garantir que les médicaments mis sur le marché, et en particulier les vaccins actuellement, aient un profil de sécurité connu et acceptable.
Déclarer un effet indésirable
Tout d'abord, qu'est-ce qu'un effet indésirable ? L'ANSM donne la définition suivante : réaction nocive survenant chez un patient, un donneur vivant ou un receveur, liée ou susceptible d'être liée à un produit ou à une activité mentionnés aux articles R.1211-29 et R.1211-30 du Code de la santé publique.
Exemples : allergie à un PTA (produit thérapeutique annexe), un excipient entraînant fièvre, frissons, ou douleur, érythème au site d'injection, kératite après greffe de cornée suite à une contamination du milieu de conservation.
Vous pouvez également consulter la définition que l'on trouve sur le site du Ministère des solidarités et de la santé et visible ci-dessous.
Pour déclarer un effet indésirable, plusieurs possibilités s'offrent à vous :
- Parler de l'effet indésirable ressenti à un professionnel de santé
- Le déclarer sur www.signalement-sante.gouv.fr, le portail de déclaration en ligne des événements sanitaires indésirables
- Le déclarer à un Centre Régional de Pharmacovigilance (CRV) dont la liste est ici. Il en existe 31 en France.
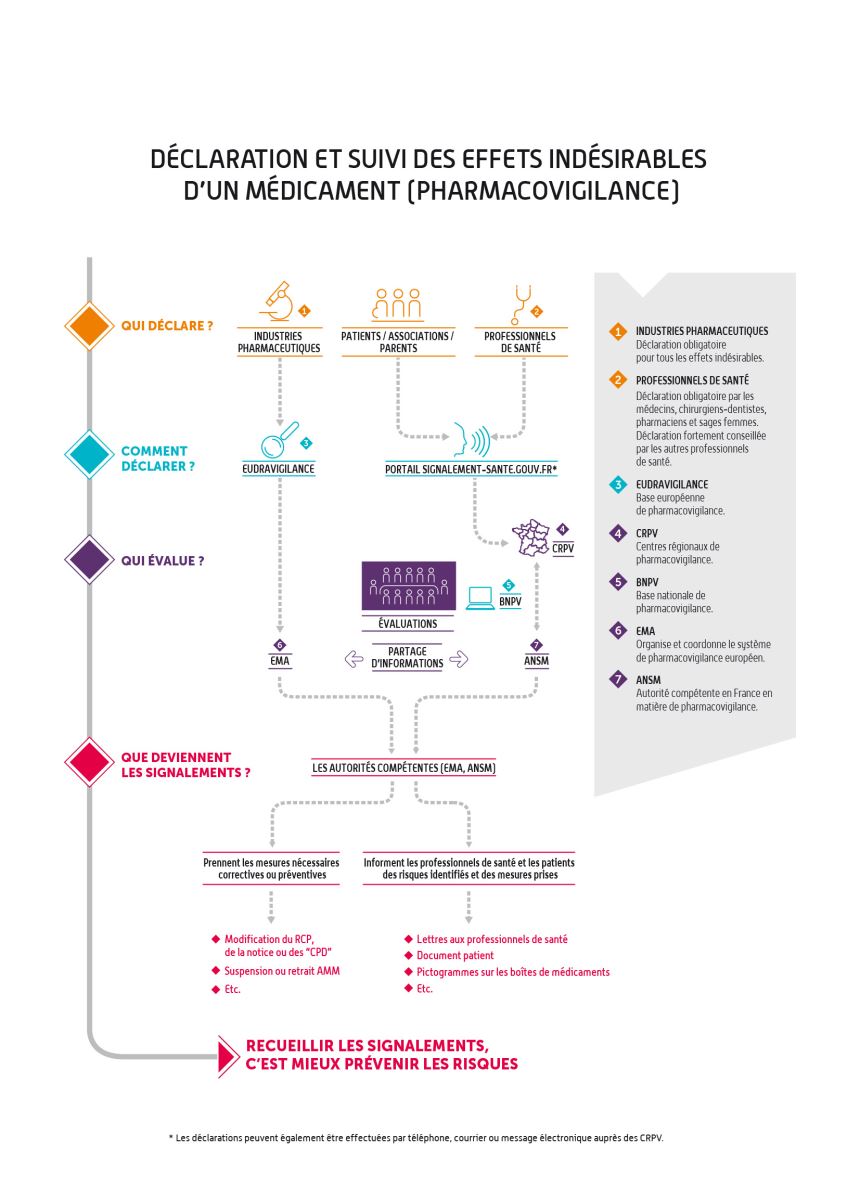
Le shéma ci-dessous vous résume le fonctionnement de la pharmacovigilance :
Pour en savoir plus, vous pouvez consulter le guide ci-dessous mais aussi visiter le site de l'ANSM.